PARA INICIARMOS!
LISTA DE EXERCÍCIOS
1-ENTRE OS MODELOS ATÔMICOS DE THOMSON E RUTHERFORD-BOHR, O QUE HÁ DE DIFERENTE ENTRE SUAS IDEIAS?
Resposta: Na ideia de Thomson ele indicou a presença de cargas elétricas, já no modelo de Rutherford-Bohr foi indicada a presenças de cargas organizadas em estruturas chamadas núcleo e eletrosfera (dividida em camadas).
Resposta: Na ideia de Thomson ele indicou a presença de cargas elétricas, já no modelo de Rutherford-Bohr foi indicada a presenças de cargas organizadas em estruturas chamadas núcleo e eletrosfera (dividida em camadas).
2-COMO SE CHAMA E COMO SE ORGANIZA A ESTRUTURA ONDE SE CONCENTRAM OS ELÉTRONS DE UM ÁTOMO?
Resposta: Elestrofera dividida em camadas K,L,M,N,O,P,Q
3- ESQUEMATIZE E INDIQUE COMO SÃO DIVIDIDOS OS ELÉTRONS EM CAMADA S ELETRÔNICAS.


4- INDIQUE O VALOR DA MASSA ATÔMICA, PRÓTONS E NEUTRONS DE TODOS OS ELEMENTOS QUÍMICOS DA TABELA PERIÓDICA ABAIXO:
OBSERVAÇÃO IMPORTANTE: ORGANIZE TODOS OS DADOS EM UMA TABELA, COM O NOME DO ELEMENTO, MASSA ATÔMICA, NÚMERO DE PRÓTONS E NÚMERO DE NEUTRONS.
Resposta:
Você deverá construir uma tabela e a parte mais difícil disso será encontrar o número de neutrons:
Resposta:
Você deverá construir uma tabela e a parte mais difícil disso será encontrar o número de neutrons:
VALOR DA MASSA ATÔMICA (NÚMERO MAIOR)
-
NÚMERO DE PRÓTONS (NÚMERO MENOR)
=
NÚMERO DE NEUTRONS
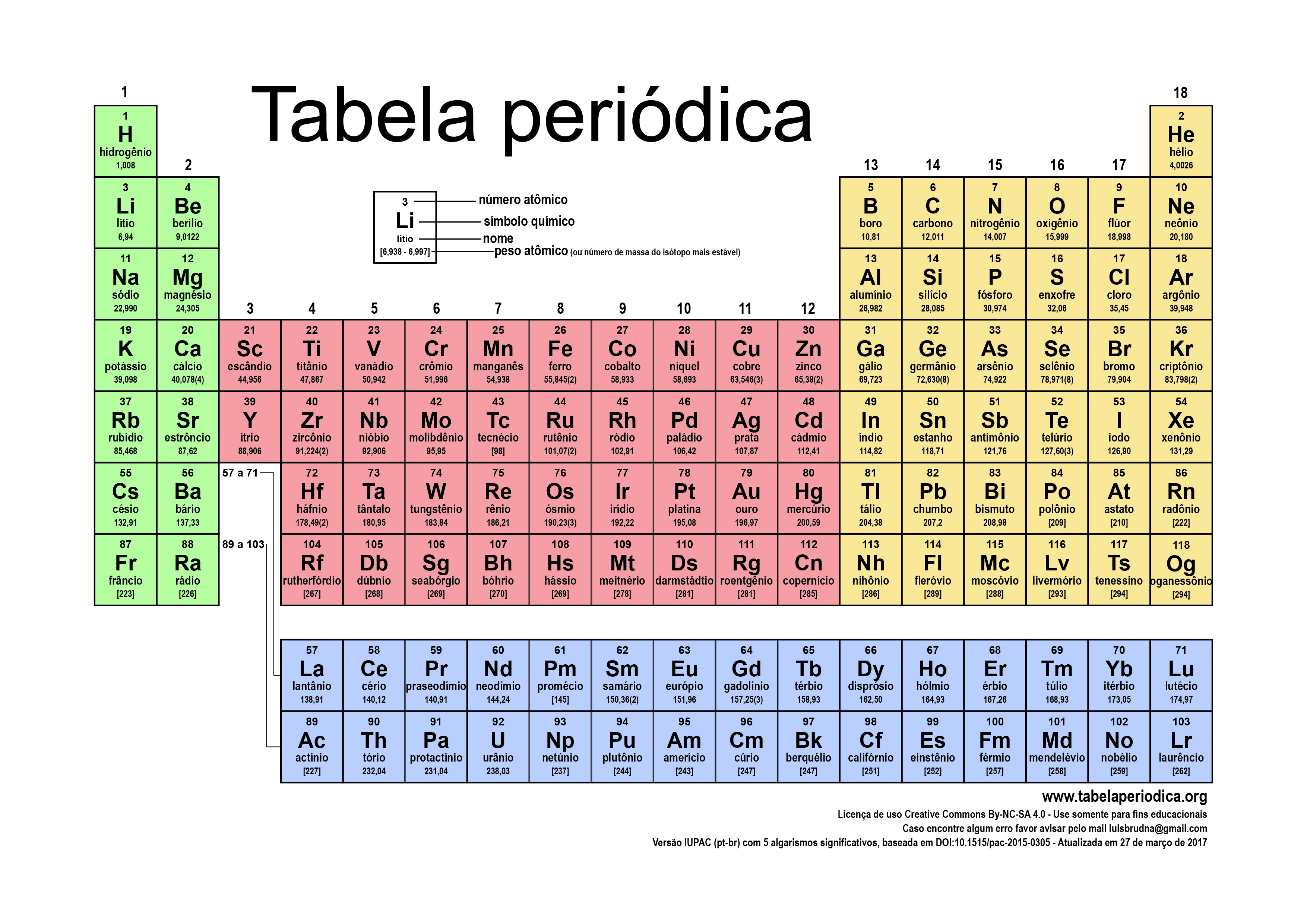
5- CONSULTANDO O NÚMERO DE ELÉTRONS NA TABELA PERIÓDICA, FAÇA A DISTRIBUIÇÃO NAS CAMADAS ELETRÔNICAS (UTILIZANDO O MODELO DE TABELA DO SEU CADERNO) DOS ELEMENTOS QUÍMICOS ABAIXO:
SÓDIO - Na
CÁLCIO - Ca
CARBONO - C
OXIGÊNIO - O
POTÁSSIO - K
HIDROGÊNIO - H
FLÚOR - F
FÓSFORO - P
CLORO - Cl
FERRO - Fe
HÉLIO - He
XENÔNIO - Xe
IODO - I


RESPOSTA: SIGA O MODELO INDICANDO A CAMADA E NÚMERO DE ELÉTRONS PRESENTE NELA ISSO PARA CADA ELEMENTO CONSULTANDO A TABELA PERIÓDICA DA QUESTÃO ANTERIOR.

RESPOSTA: SIGA O MODELO INDICANDO A CAMADA E NÚMERO DE ELÉTRONS PRESENTE NELA ISSO PARA CADA ELEMENTO CONSULTANDO A TABELA PERIÓDICA DA QUESTÃO ANTERIOR.
